Введите слово или словосочетание на любом языке 👆
Язык:
Перевод и анализ слов искусственным интеллектом ChatGPT
На этой странице Вы можете получить подробный анализ слова или словосочетания, произведенный с помощью лучшей на сегодняшний день технологии искусственного интеллекта:
- как употребляется слово
- частота употребления
- используется оно чаще в устной или письменной речи
- варианты перевода слова
- примеры употребления (несколько фраз с переводом)
- этимология
Что (кто) такое Стеклообразное состояние - определение
Найдено результатов: 218
Стеклообразное состояние
низкомолекулярных соединений, твёрдое аморфное состояние вещества, образующееся при затвердевании его переохлажденного расплава. Обратимость перехода из С. с. в расплав и из расплава в С. с. является особенностью, которая наряду со способом получения отличает С. с. от других твёрдых аморфных состояний (См. Аморфное состояние), в частности от тонких аморфных металлических плёнок. Постепенное возрастание вязкости расплава препятствует кристаллизации (См. Кристаллизация) вещества, т. е. переходу к твёрдому состоянию с наименьшей свободной энергией. Например, коэффициент динамической вязкости такого стеклообразующего вещества, как 5102 при температуре плавления Тпл= 1710°С составляет 107,7 пз (для воды при Тпл = 0 °С -0,02 пз). Переход расплава в С. с. (процесс стеклования (См. Стеклование)) характеризуется некоторым температурным интервалом. С. с. метастабильно; переход вещества из С. с. в кристаллическое является фазовым переходом 1-го рода.
В С. с. может находиться значительное число неорганических веществ: простые вещества (S, Se, As, Р); окислы (В2О3, SiO2, GeO2, As2O3, SbO3, FeO2, V 2O5), водные растворы H2O2, H2SO4, H3PO4, HClO4, H2SeO4, H2CrO4, NH4OH, КОН, HCl, LiCl: халькогениды мышьяка, германия, фосфора; некоторые галогениды и карбонаты. Многие из этих веществ составляют основу сложных стекол (См. Стекло).
Вещество в С. с. представляет собой жёсткую систему атомов и атомных групп, связь между которыми в большей или меньшей степени определяется ковалентными взаимодействиями. Дифракционные методы исследования (Рентгеновский структурный анализ, Электронография, Нейтронография) позволяют определить упорядоченность в расположении соседних атомов (ближний порядок, см. Дальний порядок и ближний порядок). Измеряя радиусы дифракционных максимумов и их интенсивности, строят т. н. кривую радиального распределения. Максимумы этой кривой соответствуют межатомным расстояниям, а площадь, ограниченная максимумами, даёт информацию о среднем числе атомов, ближайших к данному.
Вещества в С. с. изотропны, хрупки, имеют раковистый излом при сколе и (в зависимости от состава) прозрачны в некоторых областях спектра (видимой, инфракрасной, ультрафиолетовой, рентгеновской и γ-лучей). Механические напряжения (из-за плохого отжига) и неоднородность структуры вещества в С. с. являются причиной двойного лучепреломления (См. Двойное лучепреломление), которое в силу вызывающих его неконтролируемых факторов нестабильно и является "вредным" в оптической технике. Однако применение находит двойное лучепреломление, вызываемое воздействием электрических и магнитных полей (см. Керра эффект). Практически все стекла слабо люминесцируют (см. Люминесценция). Для усиления этого эффекта в них добавляют активаторы - редкоземельные элементы, уран и др. Используя накачку (См. Накачка) и специально подобранные активаторы, получают мощное когерентное излучение (см. Лазер). Вещества в С. с., как правило, диамагнитны, значительные примеси окислов редкоземельных металлов делают вещества в С. с. парамагнитными. Из некоторых стекол специального состава получают ферромагнитные материалы (например, некоторые Ситаллы). По электрическим свойствам большинство стекол - Диэлектрики (силикатные стекла), но есть большая группа веществ, обладающих в С. с. свойствами полупроводников (халькогенидные стекла, см. Полупроводники аморфные).
О С. с. полимеров см. в ст. Стеклование полимеров.
Лит.: Мотт Н., Дэвис Э., Электронные процессы в некристаллических веществах, пер. с англ., М., 1974; Аппен А. А., Химия стекла, 2 изд., Л., 1974.
Г. З. Пинскер.
СТЕКЛООБРАЗНОЕ СОСТОЯНИЕ
твердое аморфное состояние вещества, возникающее при застывании его переохлажденного расплава. В стеклообразном состоянии могут находиться лишь некоторые вещества (см. Стекло, Полимеры).
Стеклообразное состояние
Стеклообразное состояние — твёрдое аморфное метастабильное состояние вещества, в котором нет выраженной кристаллической решётки, условные элементы кристаллизации наблюдаются лишь в очень малых кластерах (в так называемом «среднем порядке»). Обычно это смеси (переохлаждённый ассоциированный раствор), в которых создание кристаллической твёрдой фазы затруднено по кинетическим причинам.
Существенное состояние
Суще́ственное состоя́ние — это такое состояние цепи Маркова, покинув которое, она всегда может в него вернуться.
АГРЕГАТНЫЕ СОСТОЯНИЯ
СОСТОЯНИЕ ОДНОГО И ТОГО ЖЕ ВЕЩЕСТВА В ОПРЕДЕЛЁННОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
Агрегатные состояния; Агрегатное состояние вещества; Фазовое состояние; Состояния вещества; Состояния материи; Агрегатные состояния вещества
вещества , состояния (фазы) одного и того же вещества (напр., воды, железа, серы), переходы между которыми сопровождаются скачкообразным изменением ряда физических свойств (плотности, энтропии и др.). Обычно рассматривают газообразное, жидкое и твердое агрегатные состояния (иногда еще плазменное). Существование у вещества нескольких агрегатных состояний обусловлено различиями в тепловом движении его молекул (атомов) и в их взаимодействии (см. Газ, Жидкость, Твердое тело, Плазма).
МЕТАСТАБИЛЬНОЕ СОСТОЯНИЕ
ТЕРМИН ОБОЗНАЧАЮЩИЙ СОСТОЯНИЕ СТАБИЛЬНОСТИ
Метастабильное состояние (в термодинамике); Метастабильное состояние квантовых систем; Неравновесная система; Метастабильность; Квазистационарное состояние
относительно устойчивое состояние системы, из которого она может перейти в более устойчивое состояние под действием внешних факторов или самопроизвольно (в последнем случае вероятность перехода значительно меньше, чем для нестабильного состояния). Пример метастабильного состояния в термодинамике - жидкость в состоянии перегрева или переохлаждения; метастабильное состояние в квантовой механике - возбужденные состояния атомов, молекул или атомных ядер, в которых они могут находиться длительное время.
Агрегатные состояния
СОСТОЯНИЕ ОДНОГО И ТОГО ЖЕ ВЕЩЕСТВА В ОПРЕДЕЛЁННОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
Агрегатные состояния; Агрегатное состояние вещества; Фазовое состояние; Состояния вещества; Состояния материи; Агрегатные состояния вещества
вещества, состояния одного и того же вещества (например, воды, железа, серы), переходы между которыми сопровождаются скачкообразными изменениями свободной энергии (См. Свободная энергия), энтропии (См. Энтропия), плотности (См. Плотность) и других основных физических свойств. Так, вода при нормальном давлении 101 325н/м2 = 760 мм рт. ст. и при 0°С кристаллизуется в лёд, а при 100°С кипит и превращается в пар. Следовательно, вода может существовать в твёрдом, жидком и газообразном А. с. К трём указанным А. с. вещества часто причисляют ещё плазму (См. Плазма). Существование нескольких А. с. обусловлено различиями в характере теплового движения молекул (атомов) вещества и в их взаимодействии. В газах (См. Газы) молекулы почти не взаимодействуют и движутся свободно, заполняя весь объём, в котором газ находится. У жидкостей (См. Жидкость) и твёрдых тел (См. Твёрдое тело) - конденсированных систем - молекулы (атомы) расположены близко друг от друга и взаимодействуют со значительными силами. Это приводит к сохранению жидкостями и твёрдыми телами определённого объёма. Однако характер движения молекул в жидкостях и в твёрдых телах различен, чем и объясняется различие их структуры и свойств. У твёрдых тел в кристаллическом состоянии атомы совершают лишь небольшие колебания вблизи узлов кристаллической решётки; структура этих тел характеризуется высокой степенью упорядоченности - дальним порядком в расположении атомов (см. Дальний порядок и ближний порядок). Тепловое движение молекул жидкости представляет собой сочетание малых колебаний около положений равновесия и частых перескоков из одного положения равновесия в другое. Последние и обусловливают существование в жидкостях лишь ближнего порядка в расположении молекул (атомов), а также свойственные жидкому состоянию подвижность и текучесть.
Плазму выделяют в особое А. с. вещества в связи с тем, что заряженные частицы плазмы, в отличие от нейтральных молекул обычного газа, взаимодействуют друг с другом на больших расстояниях. Этим объясняется ряд своеобразных свойств плазмы.
Переходы из более упорядоченного по структуре А. с. вещества в менее упорядоченное могут происходить как скачком при определённых температуре и давлении (см. Плавление, Кипение), так и непрерывно (см. Фазовый переход). Возможность непрерывных переходов (например, жидкости в пар - см. Критические явления) указывает на некоторую условность выделения А. с. веществ. Эта условность подтверждается существованием твёрдых аморфных веществ, сохранивших структуру жидкости (см. Аморфное состояние); нескольких видов кристаллического состояния у ряда веществ (см. Полиморфизм); жидких кристаллов (См. Жидкие кристаллы); существованием у полимеров особого высокоэластического состояния (См. Высокоэластическое состояние), промежуточного между стеклообразным и жидким, и другими явлениями. В связи с этим в современной физике вместо понятия А. с. вещества пользуются более широким понятием фазы (см. Фаза в термодинамике).
Метастабильное состояние
ТЕРМИН ОБОЗНАЧАЮЩИЙ СОСТОЯНИЕ СТАБИЛЬНОСТИ
Метастабильное состояние (в термодинамике); Метастабильное состояние квантовых систем; Неравновесная система; Метастабильность; Квазистационарное состояние
Метастабильное состояние (от «через» и «устойчивый») — состояние квазиустойчивого равновесия физической системы, в котором система может находиться длительное время.
Метастабильное состояние
ТЕРМИН ОБОЗНАЧАЮЩИЙ СОСТОЯНИЕ СТАБИЛЬНОСТИ
Метастабильное состояние (в термодинамике); Метастабильное состояние квантовых систем; Неравновесная система; Метастабильность; Квазистационарное состояние
I
Метастаби́льное состоя́ние (от Мета... и лат. stabilis - устойчивый)
в термодинамике, состояние неустойчивого равновесия физической макроскопической системы, в котором система может находиться длительное время. Примерами М. с. могут служить перегретая или переохлажденная жидкость и переохлажденный (пересыщенный) пар (см. Перегрев и Переохлаждение). Жидкость, например воду, тщательно очищенную от посторонних твёрдых частичек и пузырьков газа (центров парообразования), можно нагреть до температуры, превышающей температуру кипения при данном давлении. Если в перегретой жидкости возникнут центры парообразования (или их введут искусственно), то жидкость взрывообразно перейдёт в пар - устойчивое при данной температуре состояние. В свою очередь пар, в котором отсутствуют центры конденсации (твёрдые частицы, ионы), можно охладить до температур, при которых устойчиво жидкое состояние, и получить переохлажденный (пересыщенный) пар. В природе пересыщенный водяной пар образуется, например, при подъёме нагретых у поверхности земли воздушных масс и последующем их охлаждении, вызванном адиабатическим расширением.
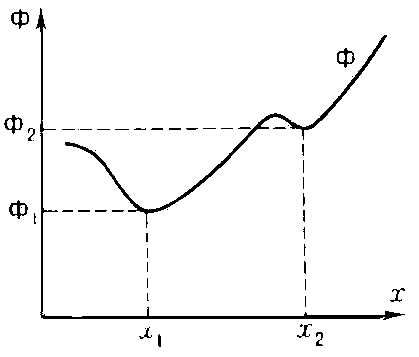
Возникновение М. с. объясняется теорией термодинамического равновесия (см. Равновесие термодинамическое). Состоянию равновесия замкнутой системы соответствует максимум энтропии (См. Энтропия) S. При постоянном объёме V и температуре Т равновесию отвечает минимум свободной энергии F (гельмгольцевой энергии (См. Гельмгольцева энергия)), а при постоянном давлении р и температуре Т - минимум термодинамического потенциала G (гиббсовой энергии (См. Гиббсова энергия)). Однако определённым значениям внешних параметров (р, V, Т и др.) может соответствовать несколько экстремумов (максимумов или минимумов) одной из перечисленных выше функций (рис.). Каждому из относительных минимумов функции F или G соответствует устойчивое по отношению к малым воздействиям или флуктуациям (См. Флуктуации) состояние. Такие состояния называют метастабильными. При небольшом отклонении от М. с. система возвращается в это же состояние, однако по отношению к большим отклонениям от равновесия она неустойчива и переходит в состояние с абсолютным минимумом термодинамического потенциала, которое устойчиво по отношению к конечным отклонениям значений физических параметров от равновесных. Т. о., хотя М. с. в известных пределах устойчиво, рано или поздно система всё же переходит в абсолютно устойчивое, стабильное состояние.
Возможность реализации М. с. связана с особенностями перехода системы из одного устойчивого состояния в другое (с кинетикой фазовых переходов (См. Фазовый переход)). Фазовый переход начинается с возникновения зародышей новой фазы: пузырьков пара в случае перехода жидкости в пар, микрокристалликов при переходе жидкости в кристаллическое состояние и т.п. Для образования зародышей требуется совершение работы по созданию поверхностей раздела двух фаз. Росту образовавшихся зародышей мешает значительная кривизна их поверхности (см. Капиллярные явления), приводящая при кристаллизации к повышенной растворимости зародышей твёрдой фазы, при конденсации жидкости - к испарению мельчайших капелек, при парообразовании - к повышенной упругости пара внутри маленьких пузырьков. Указанные факторы могут сделать энергетически невыгодным возникновение и рост зародышей новой фазы и задержать переход системы из М. с. в абсолютно устойчивое состояние при данных условиях.
М. с. широко встречаются в природе и используются в науке и технике. С существованием М. с. связаны, например, явления магнитного, электрического и упругого Гистерезиса, образование пересыщенных растворов, Закалка стали, производство стекла (См. Стекло) и т.д.
Лит.: Ландау Л. Д., Лифшиц Е. М., Статистическая физика, М., 1964; Штрауф Е. А., Молекулярная физика, М. - Л., 1949; Самойлович А. Г., Термодинамика и статистическая физика, 2 изд., М., 1955; Скрипов В. П., Метастабильная жидкость, М., 1972.
Г. Я. Мякишев.
Ф1(х1) - абсолютный минимум функции Ф (ею могут быть потенциалы F или G), Ф2(х2) - относительный минимум функции; х - переменный физический параметр (например, объём V), другие параметры постоянны.
II
Метастаби́льное состоя́ние
квантовых систем, возбуждённое состояние атомных систем (атомов, молекул, атомных ядер), которые могут существовать длительное время и, т. о., стабильны. Метастабильными являются такие возбуждённые состояния, Квантовые переходы из которых в состояния с меньшей энергией, сопровождающиеся излучением (т. е. испусканием фотонов), запрещены Отбора правилами (точными или приближёнными) и, следовательно, либо совсем не могут происходить, либо мало вероятны. Мера метастабильности состояния - его время жизни τ = 1/A, где А - полная вероятность перехода из данного состояния во все состояния с меньшей энергией. Чем меньше А, тем больше τ и тем состояние более стабильно. В предельном случае строго запрещенных переходов А = 0, τ = ∞. Обычно времена жизни для М. с. атомов и молекул составляют доли сек и сек.
Атомы и молекулы в М. с. играют важную роль в элементарных процессах, например в разрежённых газах: энергия возбуждения может длительное время сохраняться частицами, находящимися в М. с., и затем передаваться другим частицам при столкновении, что вызывает послесвечение. Процессы люминесценции (См. Люминесценция) сложных молекул связаны с наличием метастабильных молекул в триплетных возбуждённых состояниях, переходы из которых в основное синглетное состояние запрещены правилами отбора. О М. с. ядер см. Изомерия атомных ядер.
М. А. Ельяшевич.
Агрегатное состояние
СОСТОЯНИЕ ОДНОГО И ТОГО ЖЕ ВЕЩЕСТВА В ОПРЕДЕЛЁННОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
Агрегатные состояния; Агрегатное состояние вещества; Фазовое состояние; Состояния вещества; Состояния материи; Агрегатные состояния вещества
Агрега́тное состоя́ние вещества (от «присоединяю») — физическое состояние вещества, зависящее от соответствующего сочетания температуры и давления.
Википедия
Стеклообразное состояние
Стеклообразное состояние — твёрдое аморфное метастабильное состояние вещества, в котором нет выраженной кристаллической решётки, условные элементы кристаллизации наблюдаются лишь в очень малых кластерах (в так называемом «среднем порядке»). Обычно это смеси (переохлаждённый ассоциированный раствор), в которых создание кристаллической твёрдой фазы затруднено по кинетическим причинам.



![Ti]]. Ti]].](https://commons.wikimedia.org/wiki/Special:FilePath/Stohrem.jpg?width=200)

